Cardiopatías Congénitas

El complejo cianosante integrado por la estenosis o atresia de la arteria pulmonar, comunicación interventricular y acabalgamiento aórtico, junto un incipiente postnatal hipertrofia de ventrículo derecho se le encuadra dentro de las llamadas cardiopatías conotruncales, que son aquellas en las que se afectan los tractos de salida de los grades vasos, de la cual la más significativa y la que encaja con la patología final observada es la Tetralogía de Fallot que ahora definiremos.
¿Qué tipo de malformación cardiaca es la TETRALOGÍA DE FALLOT (TF)?
Para explicarlo tenemos que describir primero los fundamentos anatómicos en que se basa.
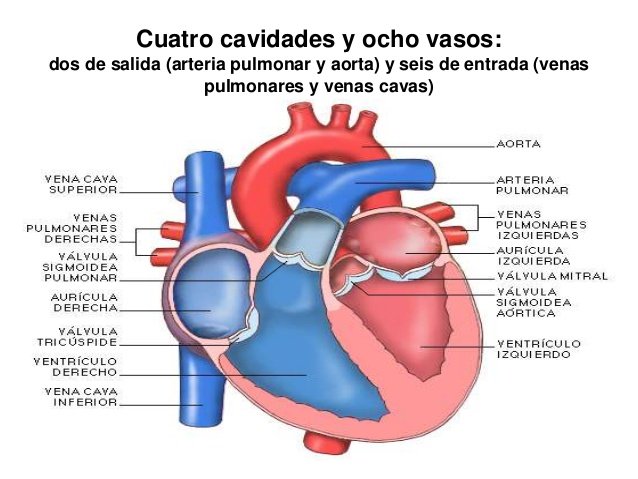
El corazón dispone de cuatro cavidades: Dos aurículas y dos ventrículos, separadas por sendas válvulas de apertura y cierre: tricúspide entre aurícula y ventrículo derecho, y mitral entre aurícula y ventrículo izquierdo. Cada aurícula y cada ventrículo se sitúan longitudinalmente conformando dos mitades, derecha e izquierda. Los ventrículos están separados a su vez por un tabique, y las aurículas por otro que en la vida fetal está permeable a través de un agujero de comunicación llamado foramen ovale.
Bajo esta distribución, la mitad del corazón integrada por aurícula y ventrículo derecho vehicula la sangre venosa que le llega de las venas cava, pobre en oxígeno, y la dirige a los pulmones a través de la arteria pulmonar. La mitad izquierda: aurícula y ventrículo izquierdo, recibe sangre oxigenada de los pulmones a través de las venas pulmonares y la reparte por el organismo a través de la arteria aorta. Todo ello supeditado a los mecanismos de bombeo propios del corazón: la sístole y la diástole.
La clave, por tanto, para este reparto de sangre estriba en dos grandes vasos que conforman los orificios de salida del corazón: Uno que parte del ventrículo derecho y acarrea la sangre venosa a los pulmones: Es la arteria pulmonar. Y otro que parte del ventrículo izquierdo que recibe la sangre ya oxigenada procedente de los pulmones y la reparte por el organismo: Es la arteria aorta.
Los orificios de entrada al corazón son las dos venas cavas, superior e inferior, que llevan a la aurícula derecha la sangre venosa procedente de cabeza y resto del cuerpo. Y las cuatro venas pulmonares que llevan a la aurícula izquierda la sangre oxigenada procedente de los pulmones.
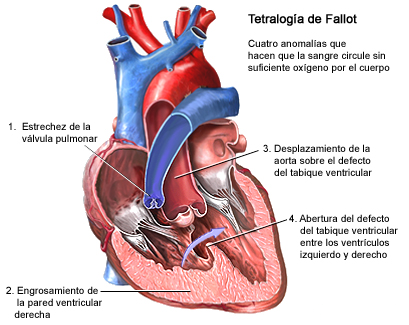
En la TETRALOGÍA DE FALLOT son esencialmente cuatro los estigmas malformativos que describió el Profesor Fallot en el año 1.888:
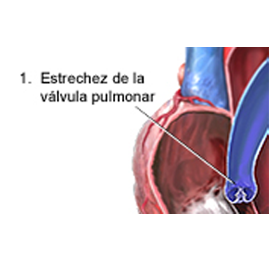
1. Estenosis de la arteria pulmonar. Que puede afectar tanto al calibre del vaso como a la válvula de comunicación con el ventrículo derecho.
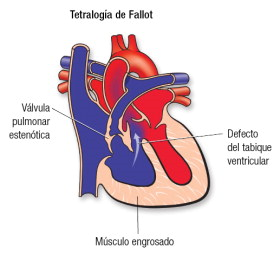

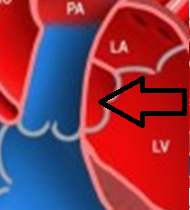
2. Comunicación interventricular. Los dos ventrículos están anormalmente comunicados por debajo de la válvula aórtica.
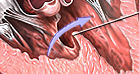
3. Cabalgamiento aórtico. Derivado del defecto anterior, el tabique interventricular presenta una mala alineación con la arteria aorta y esta sale por encima de ambos ventrículos, no lateralmente e incurvada desde el ventrículo izquierdo.
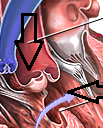
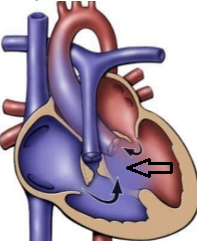
4. Hipertrofia ventricular derecha. Visible solo a partir de la vida postnatal, cuando ya se instala una estenosis crónica de la arteria pulmonar al existir respiración pulmonar. En el feto la tetralogía es realmente una trilogía.
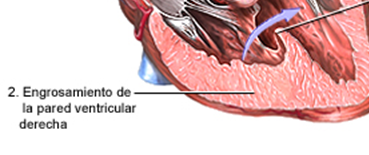
¿Qué fallo hemodinámico sucede en el recién nacido con Tetralogía de Fallot?
Para entenderlo con claridad es necesario conocer la manera en que circula la sangre en el feto, dado que aún no hay pulmones funcionantes y la circulación pulmonar, al contrario que en el adulto, es inexistente. El órgano que los sustituye se llama placenta y el oxígeno que utiliza es el producido por los pulmones de la madre.
En la placenta, el oxígeno procedente de la madre tiene paso libre desde el espacio intervelloso hacia los capilares fetales por el mayor gradiente de presión en la madre que en su hijo, y al contrario de lo que ocurre en la vida postnatal, en el feto es una vena, la vena umbilical, la que acarrea sangre oxigenada.
Esta sangre oxigenada vehiculada por la vena umbilical entra en el feto, pasa por un conducto llamado ductus venoso soslayando la circulación hepática, e ingresa en el corazón fetal en la aurícula derecha a través de la vena cava inferior. Pero una vez ahí, la dirección y velocidad del flujo sanguíneo hace que se introduzca directamente en la aurícula izquierda a través de una comunicación entre ambas aurículas, llamada foramen ovale, que solo existe en la vida fetal.
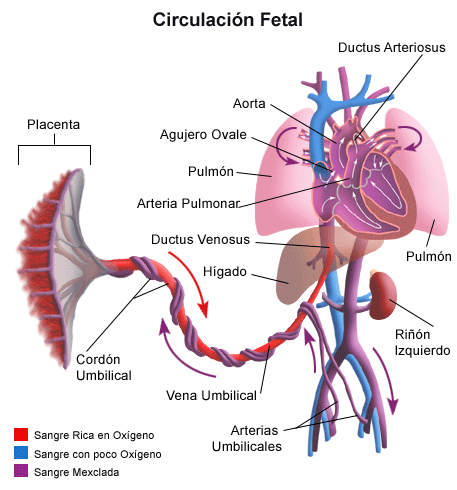
Esta sangre oxigenada y procedente de la placenta que se ha “colado” en la aurícula izquierda pasa al ventrículo izquierdo y de ahí se expande a través de la aorta ascendente hasta irrigar el cerebro.
Una vez oxigenado el cerebro y convertida en sangre venosa regresa a de nuevo a la aurícula derecha a través de la vena cava superior. Pero esta vez la dirección del flujo sanguíneo lleva una orientación y fuerza diferente y no pasa a la aurícula izquierda, sino que sigue al ventrículo derecho, ignorando el foramen ovale, y desde ahí la arteria pulmonar la dirige a los pulmones.
Ahora bien, los pulmones no son funcionantes en el feto, y la resistencia de sus vasos sanguíneos es elevada; por tanto, la sangre no circula.
Para resolver este problema existe otro conducto de comunicación, llamado ductus arteriosus – solo presente también en la vida fetal y cerrado tras el nacimiento al igual que el foramen ovale – que une el tronco de la arteria pulmonar con el cayado de la arteria aorta. Gracias a este conducto la sangre que ha llegado a unos pulmones cerrados es redirigida hacia la aorta descendente, donde esta sangre que no ha podido ser oxigenada en los pulmones es vehiculada por el sistema arterial – en este caso la aorta, un hecho solo posible en el feto por su ausencia de circulación pulmonar – donde se ramificará en las dos arterias ilíacas externas de las que partirán las arterias umbilicales y de ahí a la placenta donde pasará a la madre y volverá oxigenada de nuevo. Y vuelta a empezar.
Estos cortocircuitos fetales, ductus arteriosus y foramen ovale, salvan la oxigenación del feto, sobre todo la del cerebro, hasta que los pulmones se expandan tras el nacimiento, momento en el que se cierran dando lugar a la circulación cardiopulmonar del adulto con una separación completa sangre arterial/sangre venosa.
En contra de esa NORMALIDAD, la Tetralogía de Fallot provoca una ANORMALIDAD, ya que la sangre venosa que a través de la arteria pulmonar debe partir del ventrículo derecho para oxigenarse en los pulmones, tanto por la estrechez en el calibre de la arteria, que impide bombearla con eficacia, como por la comunicación interventricular “ataja” por esta comunicación y se mezcla con la sangre oxigenada que partiendo del ventrículo izquierdo se distribuye a través de la aorta. Esto impide una oxigenación completa de la sangre circulante al mezclarse sangre venosa, no oxigenada, con sangre arterial, oxigenada, dando lugar a un individuo de aspecto cianótico con predominio de sangre venosa en su organismo, pudiéndole acarrear insuficiencia respiratoria y posteriormente fallo cardiaco y muerte.
¿Es posible diagnosticar la TF intraútero?
La prevalencia de las cardiopatías congénitas en la población general es del 0,8% representando la TF entre el 5-8% de todas ellas, siendo por tanto el 0,08 de todas las malformaciones fetales que pueden observarse. Afecta aproximadamente a 1 de cada 8.500 nacidos vivos con un ligero predominio de varones sobre mujeres. No obstante, es la más frecuente de las cardiopatías que asocian más de una lesión. Se la encuadra dentro de las llamadas cardiopatías conotruncales, que son aquellas en las que se afectan los tractos de salida de los grades vasos: Tetralogía de Fallot, Atresia pulmonar con comunicación interventricular, Transposición de grandes arterias, Doble salida del ventrículo derecho y Truncus arterioso común.
El diagnóstico prenatal es difícil cuando no se ve afectado el corte básico de las 4 cámaras, por lo que debe incidirse en:
– Valoración del eje cardíaco.
– Corte de los 3 vasos.
– Visualización correcta de los tractos de salida.
– Observación del calibre y dirección de la aorta.
Siendo especialmente útil el Doppler color cuando la comunicación interventricular es pequeña. Suele estar asociada al Síndrome de Down en un 15-20% de tales individuos, y no tiene manifestación hemodinámica en la vida intrauterina al no existir circulación pulmonar.
Respecto a las tasas de detección, las estadísticas son variables.
El estudio EUROFETUS que abarcó los diagnósticos ultrasonográficos de malformaciones en 61 unidades obstétricas europeas durante un período de 3 años (1990-1993), empleando examen ecográfico de rutina, no selectivo para malformaciones, y con la equipación existente en aquella época, en nada comparable a los equipos de alta resolución actuales, el ratio diagnóstico fue elevado para el sistema nervioso central (88,3%) y el tracto urinario (84,8%), decayendo a un porcentaje del 38,8% para el corazón y los grandes vasos, bien que sin empleo de ecocardiografía selectiva.
No obstante, la Revista Española de Ultrasonidos en Obstetricia y Ginecología (REUOG nº 1 de la Sección de Ecografía de la Sociedad Española de Ginecología y Obstetricia (SESEGO) publicaba en el año 2004 los resultados de un estudio EUROFETUS para el año 1.996 en el que elevaba el ratio diagnóstico para cardiopatías hasta el 65% para la semana 21.
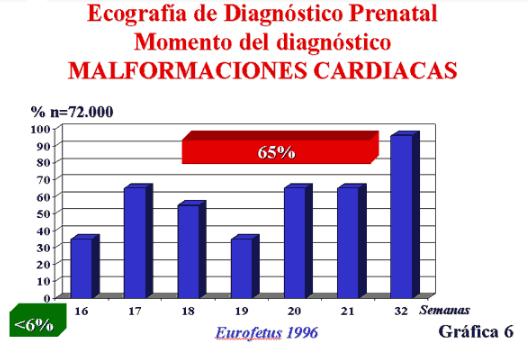
Más recientemente el Instituto Dexeus de Barcelona en un trabajo publicado en la Revista Diagnóstico Prenatal 1(on line el 22-12-2011) utilizando ecocardiografía en una población seleccionada y empleando los modernos equipos de ultrasonidos con cineloop, alta definición, sistema SRI de eliminación de ruidos y doppler color, presenta una tasa de detección de malformaciones cardiacas del 94% con un 71% de ellos obtenidos antes de la semana 23. En este mismo estudio se menciona otro nacional, de Galindo y colaboradores2, que utilizando los datos proporcionados por los hospitales para una encuesta nacional en España durante el período 2004-2006 muestra una tasa de detección prenatal total de cardiopatías congénitas del 65,7%, siendo el 52,6% obtenido ante de la semana 22.
La variabilidad en las tasas de detección de cardiopatías en los últimos 25 años es amplísima; una casuística del 27% de detección global en ecografía básica publica Mc Brien et al. en el 2009[1]; sin embargo Achiron et al. ya en 1992 presentaban una sensibilidad en la detección de cardiopatías del 48% en los casos de exploración cardíaca básica (corte de cuatro cámaras) y del 78%, cuando se realizaba una exploración cardíaca básica ampliada.
El estudio de la Clínica Dexeus, en el listado de cardiopatías congénitas diagnosticadas en el periodo a que hace referencia (2004 a 2009), obtuvieron 5 diagnósticos para la Tetralogía de Fallot lo cual representa el 4,8% de las cardiopatías, porcentaje que obedece a la casuística de presentación de esta enfermedad. Dejando solo sin diagnosticar 1 caso de TF.
Dexeus publica las indicaciones para ecocardiografía fetal y las cardiopatías que finalizaron por interrupción del embarazo:

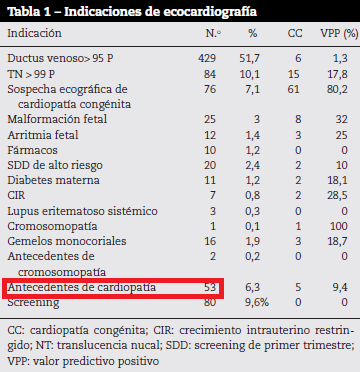
¿Cómo se realiza el Examen ecográfico del SEGUNDO TRIMESTRE?
Es un examen rutinario de aplicación universal para todas las embarazadas y junto a la ecografía de primer trimestre forma la columna vertebral en que se basa hoy día el diagnóstico de los defectos anatómicos y cromosómicos de un feto.
Por definición, Diagnóstico Prenatal se consideran las acciones diagnósticas encaminadas a descubrir un defecto congénito antes del parto. Un defecto congénito es una anomalía del desarrollo, funcional, estructural o molecular que está presente al nacer. Una malformación es aquella anomalía morfológica o estructural de un órgano o sistema. Puede ser producida por factores genéticos, ambientales o por una combinación de ambos.
El objetivo de la vigilancia y control del embarazo se centra hoy día de manera muy particular, y hasta hace poco inexistente, en la detección precoz de defectos congénitos al estar vigente una regulación legal que permite la interrupción voluntaria del embarazo con arreglo a unos plazos fijados.
Al respecto, y ayudándose de una herramienta esencial en la vigilancia del embarazo como son los exámenes ultrasonográficos, la Sociedad Española de Ginecología y Obstetricia (SEGO) publica dentro de sus Guías prácticas de asistencia la GUÍA DE LA SISTEMÁTICA DE LA EXPLORACIÓN ECOGRÁFICA DEL SEGUNDO TRIMESTRE publicada en 2015, refundida de anteriores protocolos y apoyada en el DOCUMENTO DE CONSENSO SOBRE DIAGNÓSTICO PRENATAL del año 2009.
Esta ecografía de la semana 20 compagina los plazos legales para la interrupción del embarazo con una visualización aceptable de los órganos fetales y la posibilidad de detectar anomalías mayores. Influye el órgano en el que acontezca la malformación, las características de la gestante, la experiencia del examinador y calidad del ecógrafo. Se acepta que para malformaciones mayores la tasa de detección oscila entre el 44 al 84%.
En este recuadro puede verse el ratio porcentual de estas malformaciones:
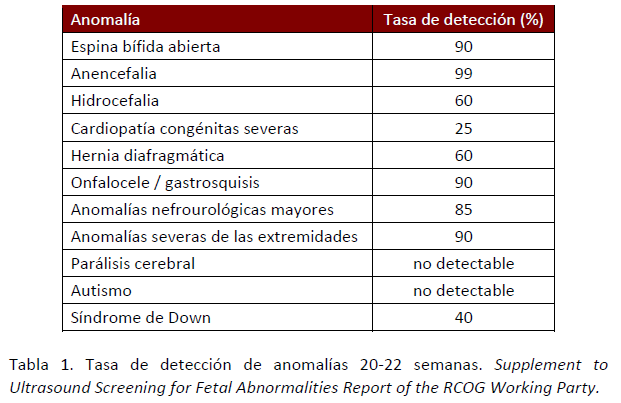
Como vemos, las cardiopatías congénitas ocupan un porcentaje pobre de detección, aunque la guía no hace distingos entre los distintos tipos de malformación.
No obstante, y en el caso que nos ocupa, independientemente de cualquier estudio porcentual la GUÍA PARA EL EXAMEN ECOGRÁFICO DEL SEGUNDO TRIMESTRE deja claro cuáles son las estructuras que han de verse en esta ecografía:

Y en lo referente al CORAZÓN el examen debe precisar: ubicación, eje, frecuencia cardiaca y tamaño del corazón. Plano de las cuatro cámaras. Tracto de salida de las grandes arterias y Corte de los 3 vasos + Tráquea.
Describimos la pauta a seguir para el estudio del corazón en el examen de rutina o cribado:
Corte de 4 cámaras (Fig. 6a). Biometría únicamente si hay sospecha de anomalía. Las estructuras a evaluar son:
a) Dos aurículas de tamaño similar, separadas por el septum primum, foramen ovale y septum secundum. El foramen oval ocupa un tercio del septo auricular y su válvula aletea hacia la aurícula izquierda, donde debe observarse la entrada de las cuatro venas pulmonares (suficiente ver dos).
b) Dos ventrículos con cavidades de similar tamaño y parecido espesor de sus paredes (observar el moderator band en el ventrículo derecho) y separados por el septo interventricular, que debe mostrase íntegro y de grosor parecido a la pared ventricular.
c) Valoración de los tabiques interauricular, aurículo-ventricular e interventricular.
Tractos de salida.
a) Tracto de salida aórtico (Fig. 6b): origen en ventrículo izquierdo, en el centro del tórax, con dirección izquierda a derecha. La aorta aparece entre las 2 válvulas aurículo-ventriculares, se continúa por detrás con la válvula mitral y por delante con el septo interventricular (porción muscular y perimembranosa deben estar integras) y sigue un trayecto cruzado respecto a la arteria pulmonar. La válvula tiene una apertura normal, con flujo normal y su tamaño es similar o algo menor que el de la arteria pulmonar.
b) Tracto de salida pulmonar (Fig. 6c): origen en ventrículo derecho (moderator band), más anterior en el tórax, con dirección derecha a izquierda y trayecto cruzado con la aorta. La válvula tiene una apertura normal, con flujo normal y su tamaño es similar o algo mayor que el de la aorta. Siempre se bifurca y deben identificarse las ramas pulmonares (la izquierda se continúa con el ductus arterial) (Fig. 7a).
Corte de 3 vasos/3 vasos-tráquea (Fig. 7b y c):
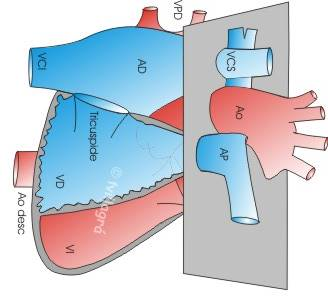
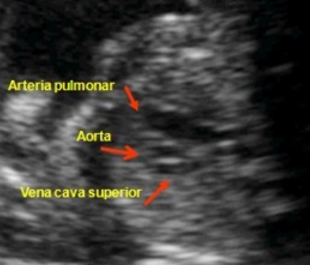
Debe valorase el número, tamaño, alineación y disposición de los 3 vasos. De izquierda a derecha y de anterior a posterior, bien alineados y de espesor decreciente aparece el corte de 3V: arteria pulmonar, aorta y vena cava superior y basculando discretamente la sonda se llega al corte de 3VT, manteniéndose la alineación y tamaño de los vasos, que adoptan una morfología en “V” y observándose la conexión de la arteria pulmonar a nivel del ductus con la aorta descendente a nivel del istmo (parte inferior de la “V”). La tráquea, econegativa, se sitúa a la derecha de la rama aórtica de la V y por detrás de la vena cava superior. El Doppler mostrará flujo anterógrado en ambos vasos, que codificarán de igual color.
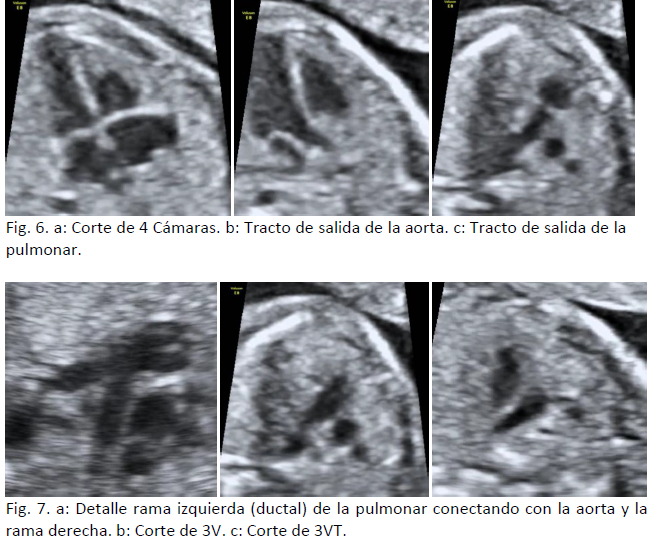
Es conveniente aplicar el Doppler para observar el flujo aurículo-ventricular de los tractos de salida que debe ser anterógrado y unidireccional sin regurgitación.
¿Qué es una ECOCARDIOGRAFÍA FETAL y cuándo se hace?
La ecocardiografía fetal es la evaluación minuciosa mediante ultrasonidos del sistema cardiovascular fetal. Es una exploración que requiere experiencia por parte del explorador, así como conocimiento de la anatomía normal y anormal del corazón y de su fisiología. Es indispensable contar con un equipo de ultrasonidos de alta definición.
En general debe realizarse una ecocardiografía fetal cuando la suma de factores de riesgo sugiere una probabilidad de cardiopatía superior a la de la población general.
Cuenta entre sus Indicaciones:
Maternas:
– Historia familiar de cardiopatías o síndromes que cursan con cardiopatía.
– Diabetes materna o enfermedades metabólicas que conllevan riesgo de cardiopatía fetal.
– Enfermedades autoinmunes como el lupus eritematoso.
– Exposición a teratógenos como fármacos antiepilépticos, anfetaminas, litio, etc.
– Infecciones maternas como la varicela, rubéola, citomegalovirus, toxoplasmosis, etc.
– Radiaciones.
– Toxicomanías.
Fetales.
– Anomalías extracardíacas.
– Anomalías cromosómicas
– Sospecha de cardiopatía en la ecografía de cribado convencional.
– Arritmias fetales.
– Retardos del crecimiento intrauterino (CIR), especialmente en su forma precoz y simétrica.
– Hidramnios.
– Hidropesía no inmune.
– Gestación múltiple, especialmente monocigótica.
– Translucencia nucal aumentada (TN > percentil 99).
En la actualidad, la resolución de las sondas transvaginales combinando la con la vía abdominal permiten una valoración precoz morfológica y funcional del corazón fetal entre las 12 y las 17 semanas cuando existen factores de riesgo relevantes para sospechar una cardiopatía congénita. Esta combinación ofrece una mayor resolución y precocidad diagnóstica, con una sensibilidad global del 60% en la detección de cardiopatías mayores. Cualquier detección o exclusión por esta técnica precoz ha de ser posteriormente corroborada en la ecografía de la semana 20.
¿Cómo se realiza?
Son numerosos los manuales y guías de asistencia publicadas para ecocardiografía fetal, ocupando una variabilidad de habilidades técnicas propias de cada centro. Nos centraremos para describir la técnica a emplear para una correcta ecocardiografía fetal tanto en la experiencia de este perito como en las directrices que publica la International Society of Ultrasounds in Obstetrics and Gynecology (ISUOG) en su Guía de asistencia:
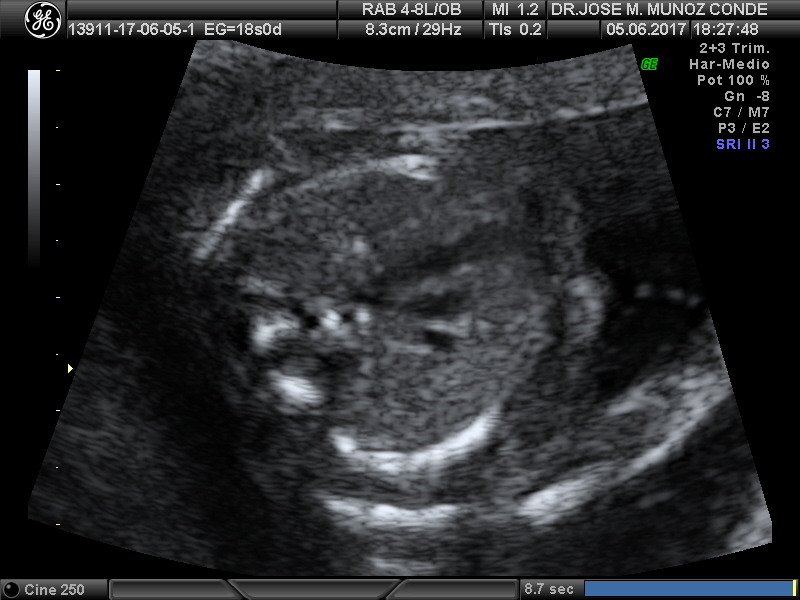
Lo primero es conseguir el corte de las CUATRO CÁMARAS, donde deberemos ver el eje del corazón, la frecuencia y ritmo cardiacos, la simetría de las cavidades, su tamaño, las conexiones valvulares, la integridad del tabique interventricular y la permeabilidad de las aurículas a través del foramen ovale cuya válvula de cierre debe abrir hacia ventrículo izquierdo.
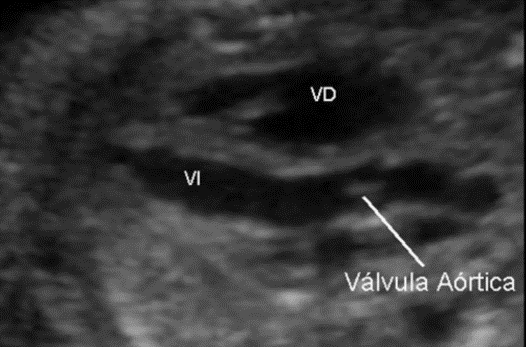
Una vez hecha esta observación buscamos ambos ventrículos; como el músculo papilar pertenece al ventrículo derecho es fácil de identificar:
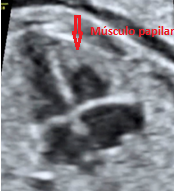
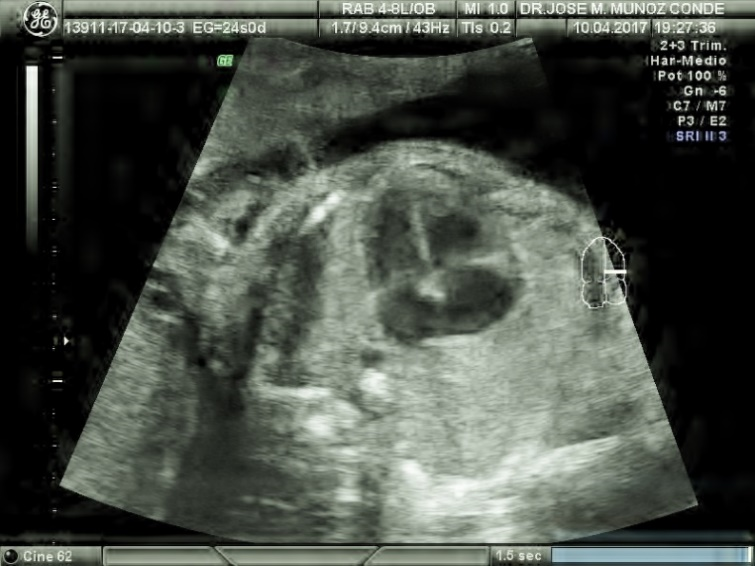
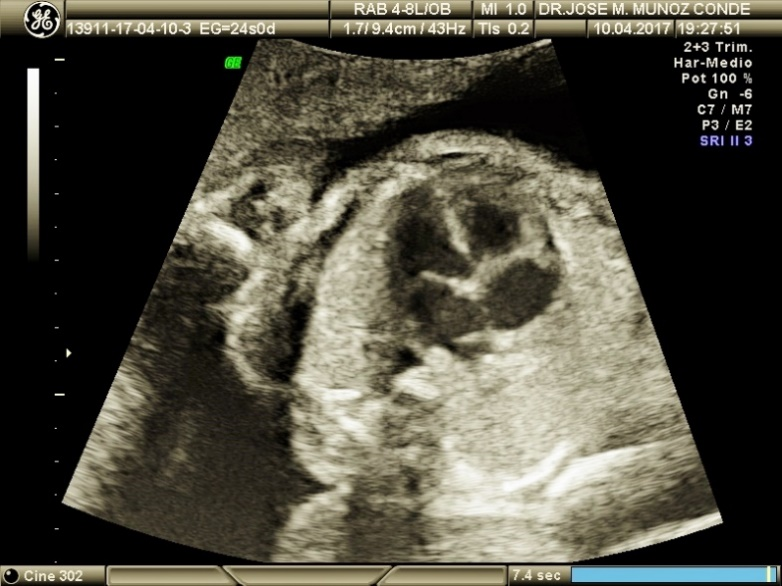
Una vez ubicado cada ventrículo se busca la salida de la aorta desde el ventrículo izquierdo e inclinando el transductor 45º a la izquierda se ve salir la arteria aorta hacia la derecha.
Este corte es también conocido como el corte de las CINCO CÁMARAS y nos confirma que la aorta sale del ventrículo izquierdo en continuidad con el tabique interventricular y se dirige correctamente hacia la derecha. Puede medirse su calibre y la dirección del flujo mediante doppler.
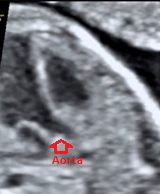
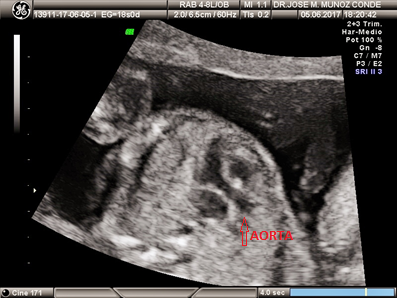
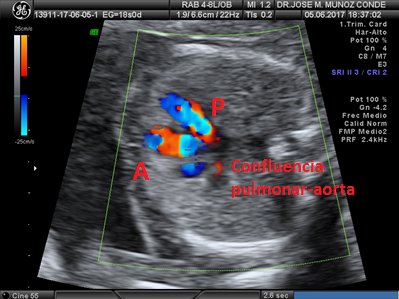
Yéndonos a continuación al ventrículo derecho y a la salida de la arteria pulmonar el transductor se inclina 45º a la derecha y la arteria pulmonar aparecerá incurvándose hacia nuestra izquierda.
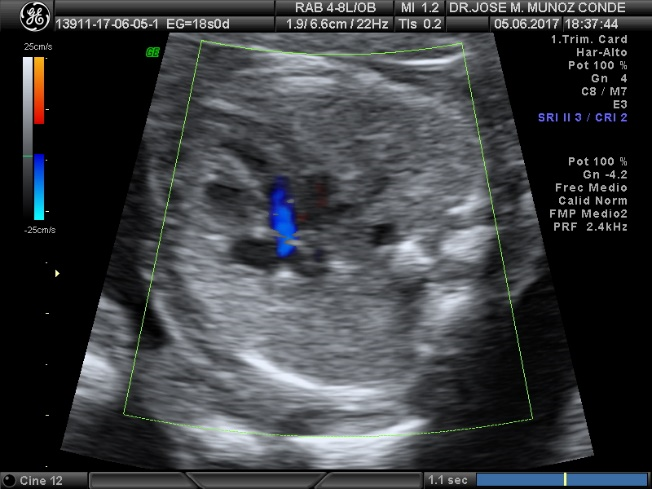
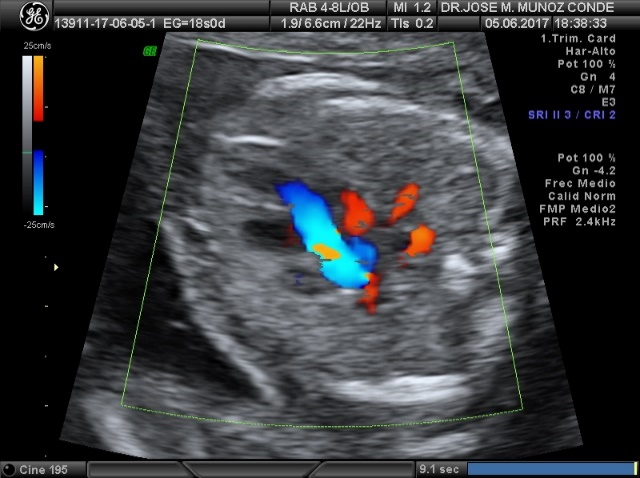
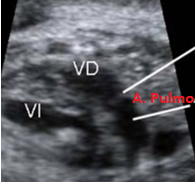
Es el momento de comprobar el entrecruzamiento de aorta y pulmonar, una saliendo de ventrículo izquierdo para incurvarse en el arco aórtico y dar lugar al plexo braquiocefálico, y la otra saliendo del ventrículo derecho se bifurca en las dos ramas del tronco pulmonar:
Ejemplo:
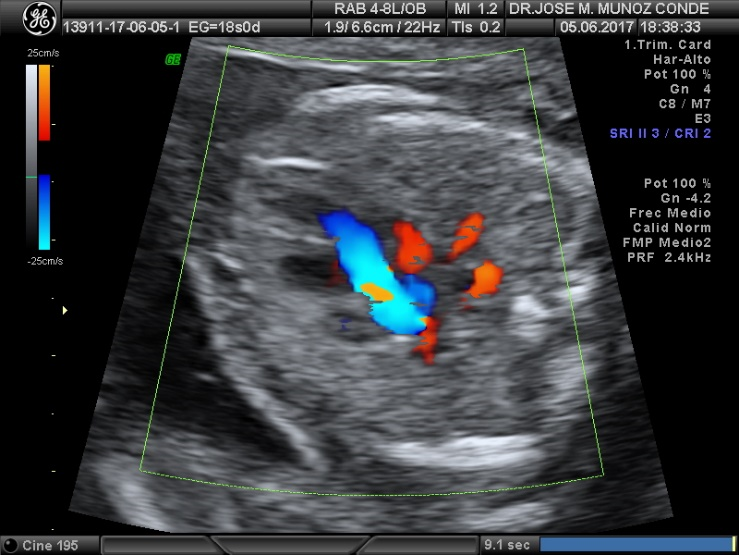
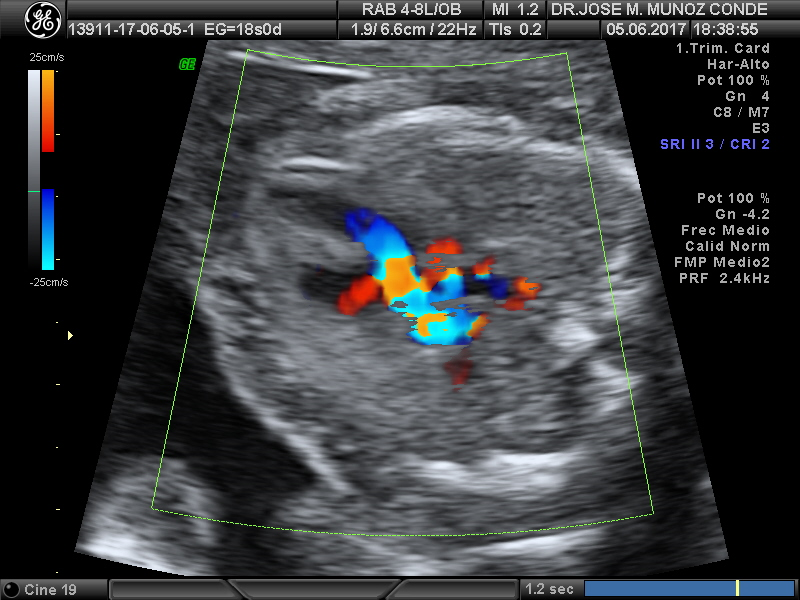
Otro corte estándar en la visualización del corazón fetal es el corte de las TRES VASOS, que realizado a nivel del mediastino superior puede incluir también la tráquea.
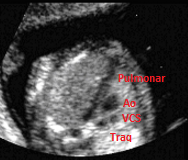
Este corte secciona horizontalmente la arteria pulmonar, aorta y vena cava superior a un nivel por encima del corazón. Sus diámetros deben ser decrecientes, el mayor corresponde al tronco pulmonar y el menor a la vena cava superior. Cualquier anomalía en el número de estos vasos, en su disposición espacial o sus tamaños relativos debe hacernos sospechar la existencia de una cardiopatía congénita, y en el caso de la TGA es muy relevante, como ahora veremos.
¿Cuáles son las diferencias cuando existe una Tetralogía de Fallot?
1. Desviación marcada del eje cardiaco hacia la izquierda
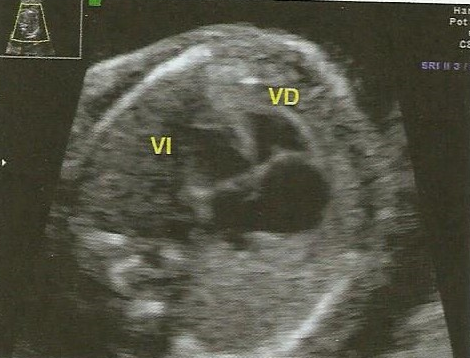
Eje cardiaco desviado a la izquierda en un ángulo mayor de 45°
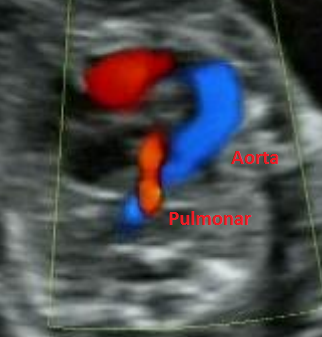
Puede verse el calibre normal de la aorta y el estrecho calibre de la arteria pulmonar
Mediante doppler se observa regurgitación del flujo sanguíneo a través de la arteria pulmonar (izquierda) en comparación con el flujo normal (derecha).
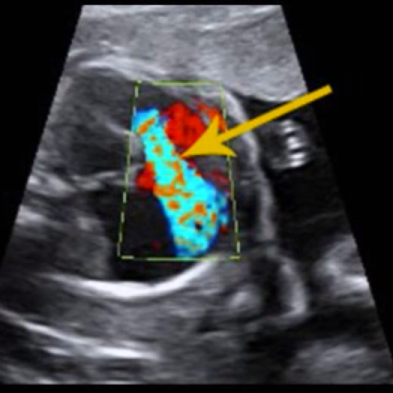
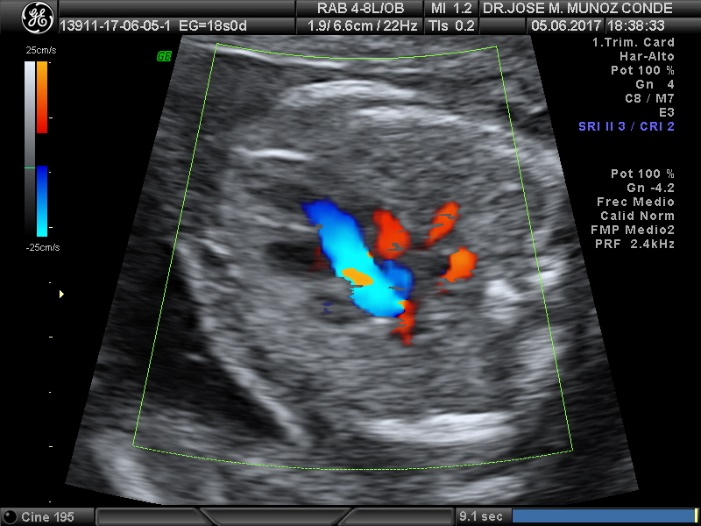
Corte anormal de los tres vasos, con ausencia del ordenamiento secuencial: arteria pulmonar, aorta, vena cava superior.
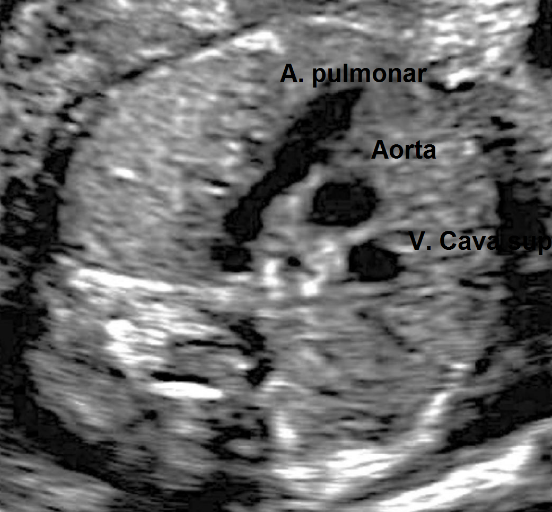
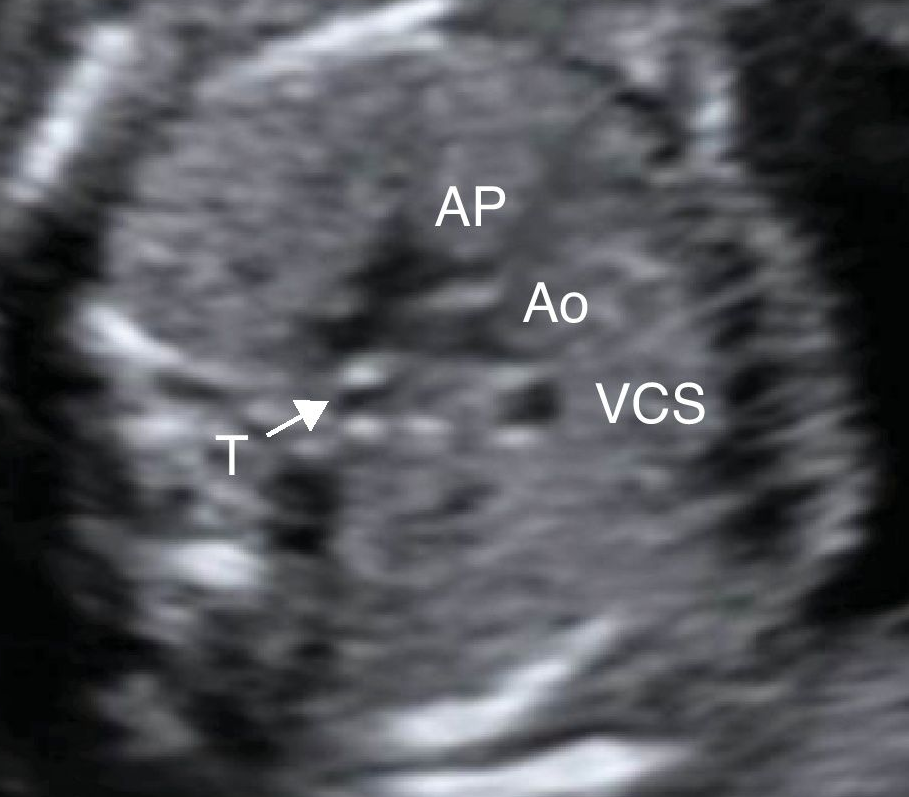
3. Comunicación interventricular
El tabique de separación entre los dos ventrículos debe estar íntegro:
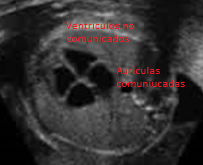
Y en las anomalías conotruncales hay una comunicación entre ambos normalmente de carácter perimembranosa; es decir, por debajo de la salida de la aorta del ventrículo izquierdo.
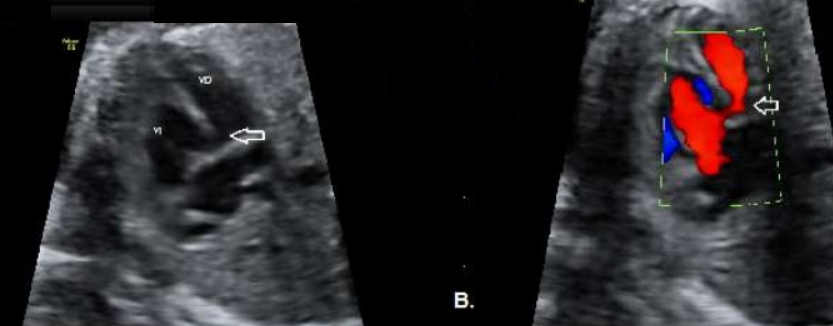
Aorta acabalgada
La aorta en vez de emerger correctamente del ventrículo izquierdo incurvándose hasta cruzarse con la arteria pulmonar:
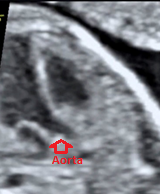
En la TF el defecto del tabique interventricular hace que la aorta quede conectada anatómicamente con ambos ventrículos, situándose por encima de ambos.
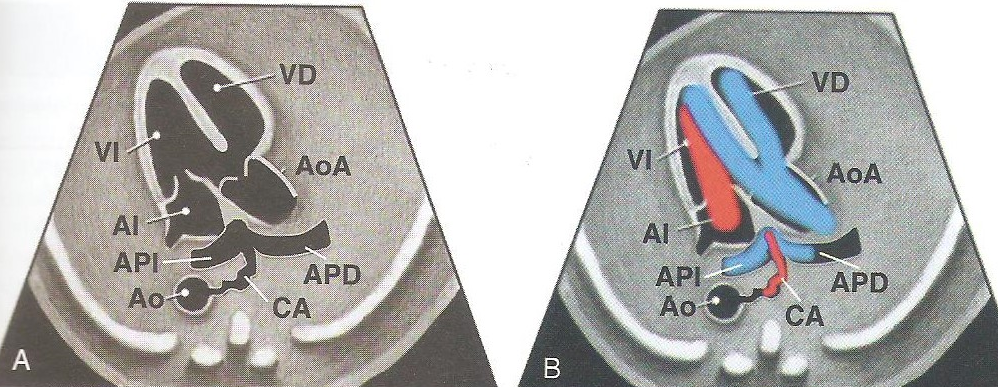
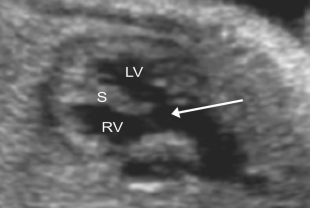
Ejemplos de aorta acabalgada (flecha) sobre los dos ventrículos:

