Síndrome de Down

¿Qué es el Síndrome de Down?
A partir de la estructuración por el Dr. Langdon Down en el año 1.866 de los rasgos característicos en los individuos afectados, que en la época dawrwiniana en que se descubrió dio lugar a la teoría de la involución étnica o salto atrás en la evolución, se define desde el año 1.959 como la presencia genética de un tercer cromosoma vinculado al par 21. Este fenómeno da lugar a una morfología y facies típica con presencia añadida de un número variable de malformaciones: principalmente cardiacas, digestivas, oculares y esquelética, y con una prevalencia, variable a su vez pero siempre, presente de retraso mental.
La incidencia global del síndrome de Down es de aproximadamente uno por cada 700 nacimientos, aunque el riesgo varía con el incremento de la edad materna, único parámetro observable en un síndrome cuya causa real es desconocida.
¿Cuáles son los métodos de que disponemos para diagnosticar una aneuploidia[1] o una malformación?
Para para diagnosticar las aneuploidias fetales más comunes se emplean lo que se llaman marcadores ecográficos y bioquímicos, bien aislados o de manera combinada según el trimestre de la gestación en el que se realicen. Se conocen como técnicas de cribado[2] y siguiendo el Protocolo de la Sociedad Española de Ginecología y Obstetricia (SEGO) Diagnóstico Prenatal de los defectos congénitos se clasifican:
1. Cribado ecográfico del I trimestre: se basa fundamentalmente en el valor de la Translucencia nucal (TN)[3]. Su tasa de detección se sitúa en el 60-65% con una tasa de falsos positivos del 5%. .
2. Cribado combinado del I trimestre: combina la TN como marcador ecográfico y dos marcadores bioquímicos del I trimestre, la β-HCG y la PAPP-A. Su tasa de detección es superior al 75%, con una tasa de falsos positivos próxima al 3%.
3. Cribado bioquímico del II trimestre mediante test doble: se basa en la cuantificación de dos marcadores bioquímicos (AFP y fβ-HCG) y no considera ningún marcador ecográfico. Su tasa de detección se sitúa alrededor del 60%, con una tasa de falsos positivos del 5%.
4. Cribado bioquímico del II trimestre mediante el test triple: se basa en la cuantificación de tres marcadores bioquímicos (AFP, β-HCG y E3) y no considera tampoco ningún marcador ecográfico. Su tasa de detección es del 60%, con una tasa de falsos positivos del 5%,
5. Cribado bioquímico del II trimestre mediante el test cuádruple: se basa en la cuantificación de cuatro marcadores bioquímicos (AFP, β-HCG, u E3 e inhibina A), sin tener en cuenta ningún marcador ecográfico. Su tasa de detección es superior al 75%, con una tasa de falsos positivos menor del 3%.
6. Cribado integrado: Combina marcadores bioquímicos y ecográficos del I trimestre (PAPP-A y TN) con marcadores bioquímicos del II trimestre (test cuádruple). El resultado del cálculo de riesgo se proporciona al final, durante el II trimestre. Su tasa de detección es superior al 75% y su tasa de falsos positivos es del 3%.
En la actualidad se utiliza el cribado combinado del I trimestre aplicado entre la 8 y 13 semanas de gestación. Puede realizarse la valoración ecográfica y bioquímica el mismo día, o hacer la determinación bioquímica entre las 8-13 semanas y la ecografía entre las 11+0 y la 13+6. Su principal ventaja es una elevada sensibilidad y la precocidad con la que permite conocer qué gestaciones son de alto riesgo, facilitando aplicar técnicas invasivas para el diagnóstico definitivo, como la biopsia corial y la amniocentesis. Este cribado se ofrece a todas las mujeres sea cual sea su edad.
El cálculo de riesgo del cribado combinado del I trimestre se establece teniendo en cuenta los valores del análisis bioquímico y el valor de la TN obtenida por ecografía. A ellos se le suman en un programa estadístico otros parámetros como el peso materno, consumo de tabaco, grupo racial de la madre, diabetes, gestación gemelar, etc. Una vez introducida la información, el programa establece un índice de riesgo principalmente para Trisomía 21. En la mayoría de los centros se incorpora también al diagnóstico la Trisomía 18 (Síndrome de Edwards) y la Trisomía 13 (Síndrome de Pateau).
En el caso del Down el rango estadístico para recomendar un estudio invasivo se sitúa en una posibilidad entre 250-300. La mayoría de los centros lo fijan en 1 entre 270: 1/270.
Cuando el riesgo es mayor; es decir, el denominador del quebrado es inferior a 270, se ofrece a la paciente la posibilidad de realizar una prueba invasiva como la amniocentesis, que consiste en entrar en la cavidad uterina mediante punción transabdominal y obtener células fetales para estudiar sus cromosomas (cariotipo).
Si el riesgo es menor; es decir, el denominador del quebrado es superior a 270 no se recomienda prueba invasiva y solo seguimiento ecográfico, quedando a criterio de los padres la realización de esta prueba invasiva basándose en su propia inquietud o en la consideración del riesgo según un criterio personal, como así lo expresa el Protocolo SEGO Diagnóstico prenatal de los defectos congénitos: “Cuando el índice de riesgo calculado a través de un programa de cribado señale que la probabilidad de aneuploidia fetal es baja, no debe considerarse una contraindicación para la realización de la técnica invasiva: Esta se podrá realizar, si la pareja así lo desea, aunque en estos casos será especialmente importante advertirles que los riesgos de la misma superan a sus posibles beneficios”.
Ecografía de Primer trimestre: ¿Qué debe verse?
Según la Guía de asistencia práctica para la Exploración ecográfica del primer trimestre que publica la SEGO ésta debe consistir en lo siguiente:
1º. Identificar el número de embriones.
2º. Diagnosticar la gestación múltiple y su tipo placentario.
3º. Comprobar y medir la frecuencia cardiaca embrionaria.
4º. Estimar la edad gestacional.
5º. Medir la Translucencia nucal.
6º. Identificar la anatomía embrionaria.
7º. Observar si existe patología uterina y de los anejos
8. La existencia se embarazos anormales como la mola hidatídica o el embarazo extrauterino.
En relación a la morfología del embrión, la Sociedad Internacional de Ultrasonidos en Obstetricia y Ginecología (ISUOG) en el año 2013 estableció los detalles anatómicos que deben observarse durante el primer trimestre. Exploración anatómica fetal entre 11ª y 13+6 semanas:
| Cabeza | Integridad ósea y de línea media. Ventrículos laterales. Plexos coroideos |
| Cara | Perfil. Hueso nasal. Órbitas con cristalinos. Labio superior. |
| Cuello | Translucencia nucal. Excluir masas-colecciones líquidas. |
| Columna | Integridad y alineación vertebral. Piel intacta. |
| Tórax | Pulmones simétricos, descartar derrames y tumores. Diafragma íntegro. |
| Corazón | Cuatro cámaras simétricas y ritmo regular. Apex izquierdo. Situs. |
| Abdomen | Estómago intraabdominal izquierdo. Riñones y vejiga. |
| Pared | Inserción umbilical normal, con pared íntegra. |
| Extremidades | 3 segmentos de los cuatro miembros: integridad, alineación, movilidad |
| Anejos | Ecoestructura placenta. Cordón con 3 v. |
Por tanto, desde un punto de vista práctico, es la ecografía del primer trimestre y posteriormente el cribado combinado bioquímico-ecográfico la vía inexcusable en cualquier embarazo para detectar precozmente los fetos afecto de alguna anomalía cromosómica o malformación orgánica.
El Documento de Consenso SEGO Diagnóstico prenatal clasifica los marcadores ecográficos sospechosos de aneuploidias en el Primer trimestre de embarazo:
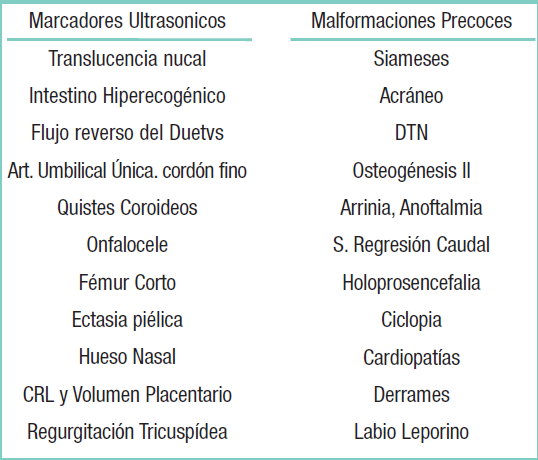
El parámetro principal es el incremento del grosor de la piel de la nuca, lo que se conoce como Translucencia nucal, y su hallazgo como marcador data del 1.985 a partir de los estudios llevados a cabo por la Dra. Beryl Benacerraf[4], refrendados posteriormente por Szabo y Gellen. Es desde entonces el modelo oro, en el que se basa la sospecha diagnóstica
Importancia de la Translucencia nucal (TN):
Ya hemos dicho que la TN es una acumulación de líquido subcutáneo bajo la piel a nivel de la nuca fetal que se encuentra aumentada en primer trimestre en las anomalías cromosómicas T 21, 18, 13, monosomía X y triploidía. Aunque el cariotipo sea normal, los fetos que presentan una translucencia nucal aumentada tienen a su vez un riesgo incrementado de cardiopatías, malformaciones esqueléticas y orofaciales, así como retraso en el desarrollo y riesgo de muerte intraútero.
¿Qué criterios deben seguirse para su medida?
Dado el impacto de la TN tanto en el cribado combinado para cromosomopatías y como marcador de otras patologías, es preceptivo obtener siempre un plano óptimo para su medición, acorde a las recomendaciones de la Fetal Medicine Foundation (FMF) recogida a su vez en el Documento de Consenso SEGO Diagnóstico prenatal:
– LCR entre 45 y 84 mm.
– Vía abdominal o vaginal.
– Feto en posición neutra.
– Sección medio-sagital, utilizando como marcadores que deben visualizarse en el mismo plano la punta ecogénica de la nariz, la forma rectangular del paladar, el diencéfalo y la TN.
– Magnificación: incluir solo cabeza y parte superior del tórax.
– Identificación de la membrana amniótica separada del feto y de la posible interposición del cordón.
– Calipers on to on.
– Reducir la ganancia.
– Medir la zona de máxima sonolucencia.
– Medir al menos 3 veces y elegir la mayor.

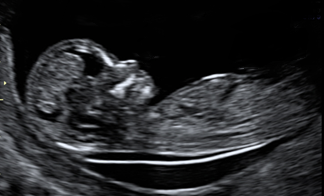
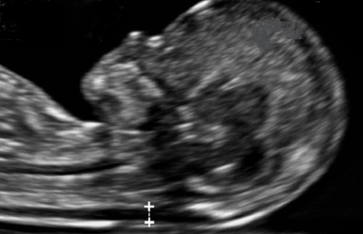
Aunque la medición de la TN no es un método diagnóstico en sí mismo, es un excelente método de selección para identificar los fetos con mayor riesgo de anomalías cromosómicas. Las tasas de detección han ido incrementando su sensibilidad, pudiendo actualmente diagnosticar el 90% de fetos con síndrome de Down con una tasa del 5% de falsos positivos.
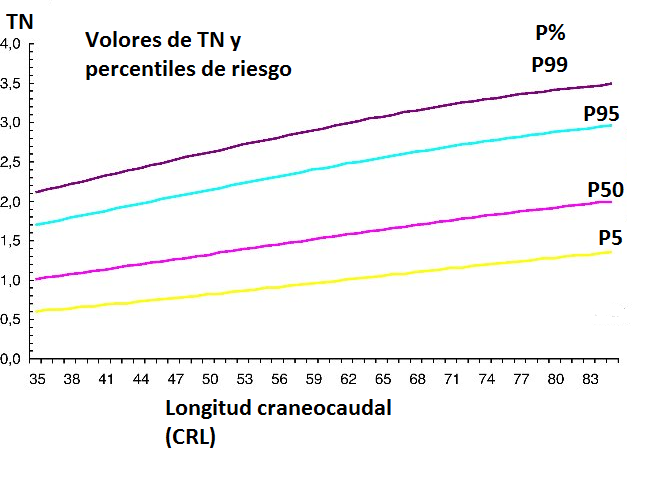
La media de la translucencia nucal aumenta de forma secuencial durante el primer trimestre, de manera que su promedio es de 1 mm para un diámetro craneocaudal del embrión (CRL) de 35 mm (10ª semana), y 2 mm para un CRL de 85 mm (17ª semana), con un valor máximo de 3 mm (>95 percentil) en la 12ª semana (CRL=55 mm). Cuando existe una medida de 3 mm en la TN, el riesgo de Trisomía 21 se multiplica por 9 y si la TN alcanza 6 mm lo multiplicaría por 18. (Documento de Consenso SEGO Diagnóstico prenatal Pag. 162 . Translucencia nucal)
[1]Se llama así a cualquier alteración o anomalía en alguno de los 23 pares de cromosomas, siendo los más frecuentes afectos los pares 21, 18 y 13. No debe confundirse con el estudio genómico: secuencia del ADN contenido en los genes de los cromosomas.
[2]Cribado es el estudio que se practica sobre un grupo poblacional para detectar una enfermedad en individuos sin signos o síntomas de esa enfermedad. Su intención es identificar enfermedades precozmente para reducir sus efectos sobre la población.
[3]Medida mediante ecografía: es el espacio sin ecos situado entre una membrana y la piel de la nuca del feto. Su medición correctamente efectuada se considera el modelo oro en el diagnóstico prenatal de la mayoría de anomalías cromosómicas, principalmente el S. Down, y algunas afecciones orgánicas como las cardiopatías.
[4] Benacerraf BR, Frigoletto FD, Lane A, Laboda RDMS: Sonographic diagnosis of Down syndrome
in the second trimester. Am J Obstet Gynecol 1985; 153:49-52.
Szabo J, Gellen J. Nuchal fluid accumulation in trisomy-21 detected by vaginosonography in
First trimester. Lancet 1990; 336:1133.

